Болезнь Ормонда или идиопатический забрюшинный фиброз представляет собой крайне редкий патологический процесс, встречаемость которого не превышает 1:200 000 человек в год. Приведенный клинический случай демонстрирует трудности диагностики нетипично протекающих редких заболеваний в практике хирурга, а также преимущества своевременно начатого лечения.
Болезнь Ормонда или ретроперитонеальный фиброз относится к редким заболеваниям, частота которого не превышает 1:200 000 человек в год. Сущность данного патологического состояния заключается в развитии воспалительного процесса неспецифического характера в жировой клетчатке забрюшинного пространства с образованием плотной фибротической ткани [1,7,10]. Впервые данное заболевание было описано французским урологом Аlbarran в 1905 году, а термин “ретроперитонеальный фиброз” был введен американцем J. К. Ormond в 1948 году [6]. В дальнейшем это заболевание приобрело множество синонимов − периренальный фасциит, фиброзный стенозирующий периуретрит, пластический периуретерит, примочеточниковый фиброз и др.
Этиологические факторы данного заболевания остаются предметом дискуссий. Существуют две основные теории заболевания − аутоиммунная и воспалительная, согласно которым выделяется первичный и вторичный ретроперитонеальный фиброз [6,7,11]. Идиопатическая форма заболевания развивается как следствие аутоиммунных процессов, что, по мнению ряда авторов, позволяет отнести ее к системным коллагенозам [13,14,15]. В развитии вторичного ретроперитонеального фиброза ведущая роль отводится различным патологическим состояниям (злокачественные новообразования, хронический гепатит, туберкулёзное поражение позвоночника и др.), приему лекарственных препаратов, воздействию облучения [2,5,6,8].
В большинстве случаев ретроперитонеальный фиброз начинается в забрюшинной клетчатке в проекции подвздошных сосудов на уровне L4-L5, постепенно распространяясь краниально и каудально к воротам почки и крестцу соответственно [11,14]. Клиническая картина заболевания зависит от степени вовлеченности забрюшинных структур в фибротический процесс − мочеточников и сосудов, в ряде случаев двенадцатиперстной и ректосигмоидного отдела толстой кишки. Лечение заключается в применении гормональных, противовоспалительных препаратов, иммунодепрессантов, генноинженерных биологических препаратов [4,9]; при наличии значимой компрессии забрюшиных структур − оперативном вмешательстве. Прогноз заболевания зависит от активности склеротического процесса и осложнений, связанных с ним (гидронефроз с исходом в хроническую почечную недостаточность, вторичная нефрогенная артериальная гипертензия, компрессия крупных сосудов) [3,12].
Приводим клиническое наблюдение из собственной практики.
Пациентка М., 44 лет, обратилась в клинику факультетской хирургии в июне 2016 г. Больной себя считает с начала октября 2015 г., когда отметила появление общей немотивированной слабости, неустойчивости настроения и периодических подъемов температуры тела до 37,2 – 37,5оС. Описанные симптомы связывала с эмоциональным стрессом, вследствие укуса энцефалитного клеща. Находилась под наблюдением в клинической инфекционной больнице им. С.П. Боткина, но клинических явлений энцефалита отмечено не было и пациентка проходила лечение у психотерапевта по месту жительства. С конца октября 2015 до января 2016 г. принимала антидепрессанты без клинического улучшения. С начала 2016 г. стала отмечать периодические боли в животе сжимающего характера без четкой локализации, иррадиировавшие в спину и паховую область. Болевые приступы длительностью от нескольких часов до суток возникали спонтанно, без конкретного триггерного механизма. К марту 2016 г. отметила усиление болей, а также урежение мочеиспускания и потемнение мочи. В связи с этим проходила обследование по месту жительства. Выполнялись общеклинические исследования, УЗИ органов брюшной полости, малого таза и почек, гастродуоденоскопия, колоноскопия, рентгенография поясничного отдела позвоночника; осмотрена гастроэнтерологом, неврологом, гинекологом и урологом. По результатам обследования выявлены: умеренный лейкоцитоз (до 12 тыс.) без сдвига лейкоцитарной формулы, повышение СОЭ, лейкоцитурия, диффузные изменения поджелудочной железы. Других клинически значимых сдвигов не обнаружено, установлен диагноз − обострение хронического цистита. Проведена антибактериальная терапия, отмечена нормализация показателей общего анализа мочи, однако положительной клинической динамики не наблюдалось − сохранялись боли в животе, дизурические явления, периодическое повышение температуры тела до субфебрильных значений. В связи с усилением болевого синдрома пациентка стала принимать обезболивающие препараты, купировавшие болевой синдром на непродолжительное время. К июню 2016 г. прием анальгетиков принял систематический характер.
В связи с отсутствием эффекта от проводимого лечения, пациентка обратилась за консультацией в клинику факультетской хирургии им. И.И. Грекова СЗГМУ им. И.И. Мечникова в июне 2016 г. с жалобами на постоянные боли в животе, преимущественно в нижних отделах с иррадиацией в спину, редкое мочеиспускание. За 6 мес. похудела на 7 кг., прием анальгетиков оказывал непродолжительный эффект. Выполнена спиральная компьютерная томография (СКТ) органов брюшной полости и забрюшинного пространства с ретроградной пневматизацией толстой кишки (14.07.2016 г). По результатам исследования данных за патологические изменения органов брюшной полости и малого таза, в том числе кишечной трубки, не выявлено. Однако стенка аорты ниже почечных артерий на 20 мм. сужена до 13 мм. до уровня бифуркации (на протяжении 99 мм.) за с чет муфтообразного мягкотканого образования с плоскостными показателями 32-47 HU, максимальной толщиной 14 мм. Описанные изменения забрюшинной клетчатки трактованы как СКТ-признаки ретроперитонеального локализованного параортального фиброматоза (болезнь Ормонда).
Учитывая компенсированный характер уродинамических нарушений (отсутствие расширения мочеточников и чашечно-лоханочной системы), оперативное лечение признано нецелесообразным, назначена гормональная терапия − преднизолон в дозировке из расчета 1 мг на 1 кг веса в сутки. С профилактической целью также назначен ингибитор протонной помпы (Омез 20 мг. 2 р/сут).
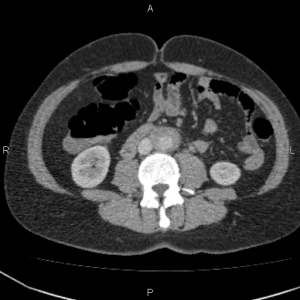
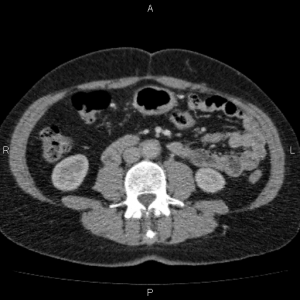
К концу второй недели лечения пациентка отметила улучшение самочувствия в виде уменьшения болевого синдрома, позволившего прекратить прием анальгетических препаратов, дизурические явления также были купированы. Прием преднизолона продолжен. 26 сентября 2016 г. выполнена контрольная СКТ органов брюшной полости и забрюшинного пространства, по результатам которой определяется выраженная положительная динамика: ранее визуализируемого параортального муфтообразного мягкотканного образования нет (рис. 1).
Рисунок A. Рисунов Б.
Результаты компьютерной томографии органов брюшной полости и забрюшинного пространства пациентки М.: А – до начала терапии кортикостероидами (14.06.2016); Б – через 2 месяца после приема преднизолона (26.09.2016) отмечается положительная динамика в виде регресса забрюшинного фибротического очага.
Пациентка повторно осмотрена в октябре 2016 г. Боли в животе и субфебрильное повышение температуры тела не беспокоят. Отмечает улучшение общего самочувствия и аппетита. Продолжает прием преднизолона. Планируется динамическое наблюдение с последующим переводом на противовоспалительные препараты.
Приведенный клинический пример демонстрирует выраженный трудности в диагностике такого редкого клинического состояния как болезнь Ормонда. Поздняя диагностика этого заболевания всегда чревата развитием необратимых склеротических изменений в забрюшинной клетчатке с компрессией трубчатых структур. В описываемом случае своевременно начатое лечение позволило добиться полного регресса фибротического процесса и клинической симптоматики, тем самым избежав оперативного вмешательства, исходы которого при болезни Ормонда неоднозначны.
Библиографический список.
1. Бондарев, В.И. Наблюдение болезни Ормонда / В. И. Бондарев, В.Г. Шлопов , А.С. Кузнецов // Клиническая хирургия. — 1984. — № 6. — C. 63-64.
2. Боровкова, Н. В. Случай ретроперитонеального фиброза (болезнь Ормонда) / Н. В. Боровкова, Л.Л. Малачиева, Н. Г. Клюев // Сибирский медицинский журнал. — 2000. — Т.15, №3. — С. 40-41.
3. Горячева, Т.С. Случай успешного оперативного лечения пациента с забрюшинным фиброзом (болезнью Ормонда) / Т.С. Горячева, Л.А. Бокерия, О.Л. Бокерия и др. // Бюллетень НЦССХ им. А.Н. Бакулева РАМН Сердечно-сосудистые заболевания. -2016. – Т. 17. № S3. – С. 110a.
4. Кныш, В.И. Синдром Ормонда в онкологической клинике / В. И. Кныш, В. С. Ананьев, В. Л. Черкес, А. Н. Элмурадов, С. Т. Мазуров // Хирургия. — 1989. — № 5. — C. 125-127.
5. Корниенко, В.И. Ретроперитонеальный фиброз (болезнь Ормонда) / В. И. Корниенко, С. Х. Аль-Шукри, А. А. Люблинская // Нефрология. — 2009. — № 3. — С.159-162.
6. Лопаткин, Н.А. — Руководство по урологии / Н.А. Лопаткин. — М.: Издательство “Медицина”, 1998. — 1024 c.
7. Мазо, Е.Б. Внешнее протезирование мочеточника при ретроперитонеальном фиброзе / Е. Б. Мазо, Г. Г. Хомерики // Урология и нефрология. — 1986. — № 3. — С. 20-25.
8. Морозов, А.В. Консервативное лечение ретроперитонеального фиброза с применением «внутреннего дренирования» почек / А. В. Морозов, С. К. Тернова // Урология и нефрология. — 1986. — № 6. — C. 63-64.
9. Парамонова, Т.И. Идиопатический ретроперитонеальный фиброз (болезнь Ормонда) наш опыт комплексной лучевой диагностики в современной кардиохирургической клинике / Т.И. Парамонова, О.С. Горностаева, А.В. Вдовкин, и др. // Диагностическая и интервенционная радиология. – 2012. – Т. 6. № 4-1 (4). – С. 103-111.
10. Эседов, Э.М. Ретроперитонеальный фиброз (болезнь Ормонда) в практике терапевта / Э.М. Эседов, Д.С. Акбиева // Вестник Дагестанской государственной медицинской академии. – 2015. – № 3 (16). – С. 63-65.
11. Corradi, D. Allopathic retroperitoneal fibrosis: Clinicopathologic features and differential diagnosis / R. Maestri, A. Palmisano, S. Bosio, P. Greco, L. Manenti // Kidney Internetional. — 2007. — Issue 72. — P. 742-795.
12. Kallen, A.J. Gadolinium-containing magnetic resonance imaging contrast and nephrogenic systemic fibrosis: A case-control study / A. J. Kallen, M. A. Jhung, S. Cheng, T. Hess, G. Turabelidze, L. Abramova // American Journal of Kidney Diseases. — 2008. — Issue 51. — P. 966-1041.
13. Marcolongo, R. Immunosuppressive therapy for idiopathic retroperitoneal fibrosis: A retrospective analysis of 26 cases / R. Marcolongo, I. M. Tavolini, F. Laveder, M. Busa, F. Noventa, P. Bassi, G. Semenzato // American Journal of Medicine. — 2004. — Issue 116. — P. 194-201.
14. Moroni, G. Longterm outcome of idiopathic retroperitoneal fibrosis treated with surgical and/or medical approaches / G. Moroni, B. Gallelli, G. Banfi, S. Sandri, P. Messa, C. Ponticelli // Nephrology Dialysis Transplantation. — 2006. — Issue 21. — P. 2485-2575.
15. Oshiro, H. Idiopathic retroperitoneal fibrosis associated with immunohematological abnormalities / H. Oshiro, Y. Ebihara, H. Serizawa, T. Shimizu, S. Teshima, M. Kuroda, M. Kudo // American Journal of Medicine. — 2005. — Issue 118. — P. 782-788.